西格玛医学洞见:人工骨临床试验设计及操作思路
分类编码:13-05-02;骨科填充和修复材料/钙盐类骨填充植入物
预期用途:手术中植入体内,用于隔离以减少直肠前部接受的辐射,或腔隙和创面的填充。
品名举例:人工骨、骨修复材料、羟基磷灰石生物陶瓷、磷酸钙生物陶瓷、β-磷酸三钙人工骨、硫酸钙人工骨、钙磷盐骨水泥、生物玻璃骨填充材料。
管理类别:Ⅲ
临床评价:临床试验或同品种
市场情况
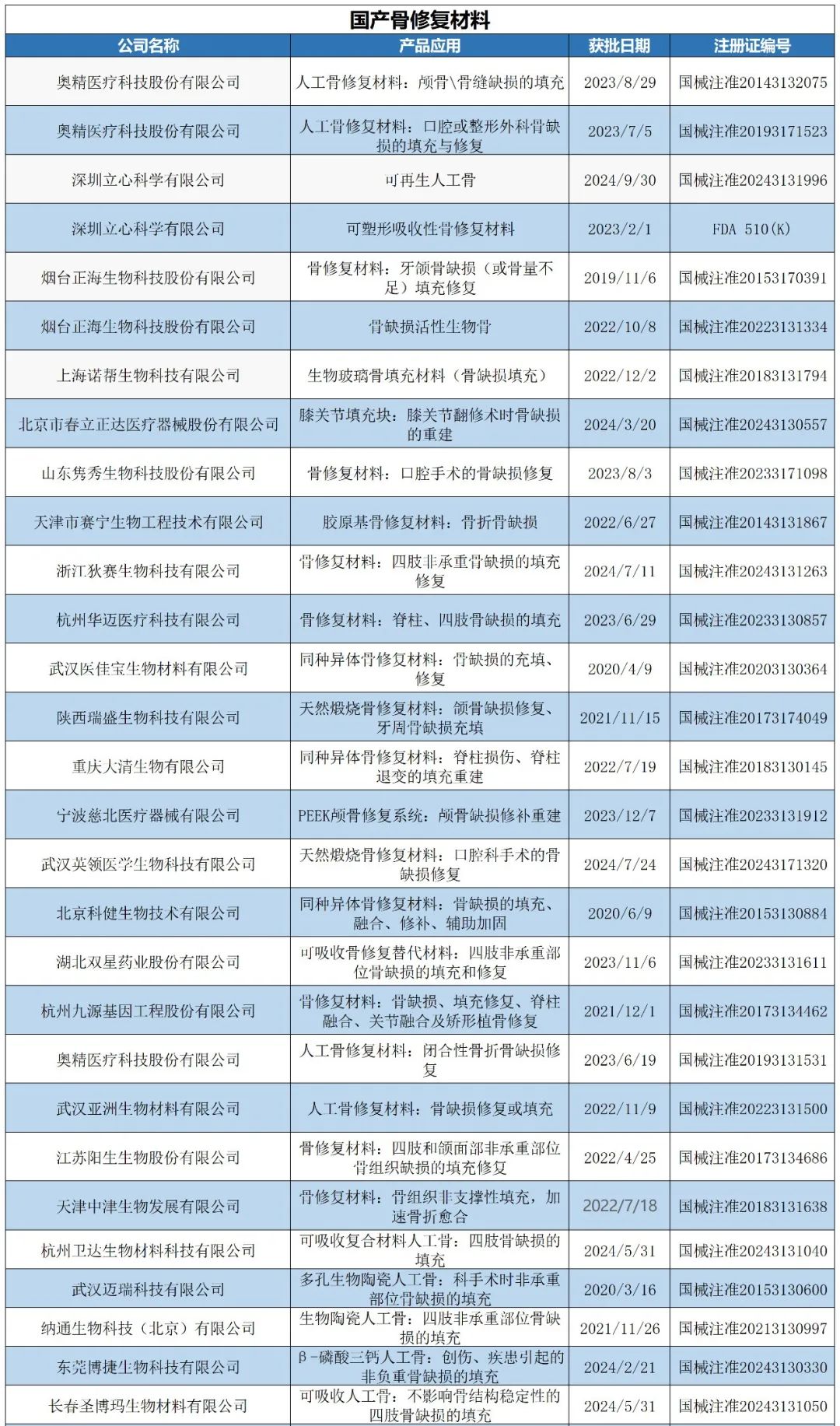
开展临床试验,需遵守《世界医学大会赫尔辛基宣言》的伦理准则和国家涉及人的生物医学研究伦理的相关规范。按照《医疗器械临床试验质量管理规范》,临床试验应当获得伦理委员会的同意。
产品分类与审批路径
[37种医疗器械临床试验设计系列]
1、西格玛医学洞见:医美类医疗器械临床试验的研究设计和操作考量
2、西格玛医学洞见:TACE栓塞微球临床试验设计
3、西格玛医学洞见:新一代生物活性骨及临床试验设计
4、西格玛医学洞见:ECMO介绍及临床试验设计
5、西格玛医学洞见:巩膜镜介绍及临床试验设计
6、西格玛医学洞见:水光针介绍及临床试验设计
7、西格玛医学洞见:银离子敷料及临床试验设计
8、西格玛医学洞见:可降解鼻窦药物支架系统介绍及临床试验设计
9、西格玛医学洞见:一文读懂角膜塑形镜及临床试验设计
10、西格玛医学洞见:一文读懂肿瘤电场治疗及临床试验设计
11、西格玛医学洞见:摄入空间占据水凝胶胶囊临床试验设计思路
12、西格玛医学洞见:一文读懂血滤,血透和血灌的区别
13、西格玛医学洞见:射频美容设备注册分类及临床试验设计操作
14、西格玛医学洞见:一文读懂胶原蛋白及临床试验设计
15、西格玛医学洞见:一文读懂机器人及临床试验设计
16、西格玛医学洞见:一文读懂人工晶状体及临床试验设计
17、西格玛医学洞见:一文读懂面部注射填充临床试验设计及操作
18、西格玛医学洞见:一文读懂青光眼引流装置及临床试验设计
19、西格玛医学洞见:一文读懂CGMS及临床试验设计
20、西格玛医学洞见:一文读懂冠脉冲击波球囊
21、西格玛医学洞见:血液透析类产品临床试验设计与操作执行
22、西格玛医学洞见:软性亲水接触镜临床试验设计与操作执行
23、西格玛医学洞见:近视弱视用激光设备临床试验及设计
24、西格玛医学洞见:射频美容设备注册分类及临床试验设计操作
25、西格玛医学洞见:一文读懂血液灌流器临床试验设计
36、西格玛医学洞见:假发及植发系统介绍及临床评价
【关于西格玛医学】
南京西格玛医学技术股份有限公司(证券代码:873450)是一家为全球创新医疗器械企业提供多个治疗领域解决方案的临床合同研究组织(CRO)。我们致力于保证卓越交付和提升客户独一无二的服务体验,凭借丰富的治疗领域全球经验,从创新产品临床开发策略,临床开发全过程实施,申报递交直至上市后监测,为客户提供全方位临床研发服务和个性化解决方案。公司涵盖的业务包括:临床试验代理、数据管理和统计、第三方稽查、器械SMO、法规注册、生产质量体系服务等科研服务。西格玛医学凭借专业的临床技术助力客户以个性化的方案解决各项问题,确保临床试验透明度和制定数据驱动决策。致力为客户缩短产品上市周期和节约研发经费并提高临床试验质量控制,推进产品市场化进程。在近二十年的发展过程中成功助力各大领域企业顺利获得二类、三类及创新产品的证书,助力各企业合规进入高端器械产业赛道,相关成果发表于《LANCET》《NEJM》等国际权刊物,并获多项国家重大奖项,为我国百姓能用上安全有效的好器械做出了重要贡献。
【联系我们】
地址:江苏省南京市鼓楼区汉中路180号星汉大厦20楼
总部电话:025-86210646
手机同微信号:13585209568/13913960642
公众号:西格玛医学
【关于西格玛医学】
南京西格玛医学技术股份有限公司(证券代码:873450)是一家为全球创新医疗器械企业提供多个治疗领域解决方案的临床合同研究组织(CRO)。我们致力于保证卓越交付和提升客户独一无二的服务体验,凭借丰富的治疗领域全球经验,从创新产品临床开发策略,临床开发全过程实施,申报递交直至上市后监测,为客户提供全方位临床研发服务和个性化解决方案。公司涵盖的业务包括:临床试验代理、数据管理和统计、第三方稽查、器械SMO、法规注册、生产质量体系服务等科研服务。西格玛医学凭借专业的临床技术助力客户以个性化的方案解决各项问题,确保临床试验透明度和制定数据驱动决策。致力为客户缩短产品上市周期和节约研发经费并提高临床试验质量控制,推进产品市场化进程。在近二十年的发展过程中成功助力各大领域企业顺利获得二类、三类及创新产品的证书,助力各企业合规进入高端器械产业赛道,相关成果发表于《LANCET》《NEJM》等国际权刊物,并获多项国家重大奖项,为我国百姓能用上安全有效的好器械做出了重要贡献。
【联系我们】
地址:江苏省南京市鼓楼区汉中路180号星汉大厦20楼
总部电话:025-86210646
手机同微信号:13585209568/13913960642
公众号:西格玛医学